Dalam ilmu kimia terdapat dua ikatan yaitu ikatan ionik dan ikatan kovalen, Ikatan ionik trjadi antara atom-atom non logam dan logam. Ikatan Kovalen terjadi diantara atom-atom nonlogam. Sedangkan valensi adalah jumlah ikatan yang dapat dibentuk suatu atom. Setiap atom suatu unsur mengandung sejumlah elektron yang sama persis dengan jumlah proton di intinya. Muatao positif proton mengimbangi muatan negatif elektron sehingga secara keseluruhan atom tersebut tidak bermuatan.
 |
|
Proton, neutron dan elektron (Gb.gcsescience.com) |
Elektron mengorbit inti dalam lapisan-lapisan ayng disebut kulit. Kulit pertama, yang paling dalam dapat menampung dua elektron. kulit kedua dapat menampung delapan elektron. Sedangkan kulit ketika dapat menampung delapan belas elektron. Baris dalam tabel periodik mendaftrakan unsur-unsur dlam urutan nomor atom, yang merupakan jumlah proton dalam sebuah atom dari suatu unsur. Setiap baris diawali dengan sebuah unsur yang hanya mempunyai satu elektron pada kulit terluarnya. Pada akhir baris itu terdapat gas mulia, yang kulit terluarnya berisi penuh elektron. Susunan ini yang disebut dengan konfigurasi, ternyata gas mulia amat stabil. Inilah mengapa gas mulia sukar bereaksi.
Valensi
Dalam reaksi kimia, ikatan terbentuk antar atom,ketika atom-atom tersebut memperoleh, kehilnagan atau berbagi elektron. Sebagai hasil perubahan-perubahan itu, setiap atom didalam suatu senyawa biasanya memiliki kulit luar yang penuh elektron. Ini merupakan konfigurasi elektron stabil dari gas mulia yang terdekat dengan setiap unsur didalam nomor atom.
Valensi sebuah unsur adalah jumlah ikatan yang harus dibuat untuk membentuk konfigurasi elektron gas mulia. Biasanya logam hanya mempunyai satu atau dua elektron dikulit terluarnya. Mereka mudah kehilangan elektron-elektron terluar tersebut sehingga kulit didalamnya akan menggantikan menjadi kulit luar yang lengkap. Sementara itu, non logam dibagian kanan tabel periodik kekurangan satu atau dua elektron agar kulit terluarnya lengkap. Inilah sebabnya mengapa mereka mudah menerima elktron-elektron dari atom-atom unsur lain. Valensi unsur-unsur ini adalah jumlah elektron yang harus diperoleh atau dilepaskan agar membentuk kulit luar dengan lengkap.
Unsur-unsur yang terdapat pada bagian tengah blok utama tabel periodik memiliki kulit terluar yang masih kekurangan tiga atau empat elektron agar kulit terluarnya lengkap. Contohnya adalah karbon, yang mempunyai empat elektron dikulit terluar, padahal kulitnya ini dapat memuat delapan elektron. Namun demikian, ia jarang menerima empat elektron lagi karena muatan negatif terlalu kuat daya tolaknya. Sebaliknya, atom karbon menumpangkan kulit terluarnya dengan kulit atom lain, dan membagikan empat elektron untuk menyusun kulit luar yang penuh. Valensi karbon adalah empat.
Ion dan Ikatan Ionik
Senyawa ionik terbentuk jika atom-atom dari dua atau lebih unsur saling bertukar elektron untuk membentuk partikel bermuatan, atau ion, dari setiap unsur. Ion-ion tersebut memiliki konfigurasi gas mulia dan muatan mereka saling mengimbangi senyawa tersebut tidak bermuatan.
 |
|
Ikatan antara Na denag Cl2 (Gb.gcsescience.com) |
Sebuah atom natrium mempunyai 11 elektron. Dua diantaranya terdapat dikulit pertamanya. Delapan elektron di kulit kedua. Kulit pertama dan kedua tersebut sudah lengkap. Satu elektron lain, elektron kesebelas, berada sendiri di kulit ketiga yang mampu menampung hingga 18 elektron.
 |
|
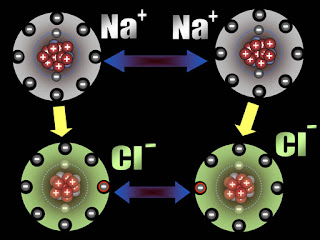
Pembentukan NaCl (Gb.gcsescience.com) |
Lain lagi dengan atom klorin yang kulit terluarnya kekurangan satu elektron. Atom klorin dapat berikatan dengan pasangan mebentuk molekul-molekul Cl2. Dalam molekul ini, sepasang elktron membuat kulit luar.
 |
|
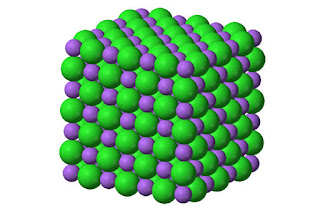
Kristal NaCl (Gb.gcsescience.com) |
Namun, bila ada natrium, atom klorin melepas ikatan itu agar memperoleh elektron sendiri-sendiri. Elektron kesebelas dari setiap atom natrium diambil, sehingga ion natrium bermuatan positif (Na+). Elektron itu diambil oleh atom klorin yang kemudian menjadi ion klorida (Cl-). Muatan yang berlawanan dari kedua atom ini meyebabkan mereka saling menarik dengan kuat. Ion-ion itu bergabung bersama dalam pola yang teratur yang disebut dengan kisi-kisi atau lattice kristal.
 |
|
Reaksi antara Logam Natrium denga gas Klorin (Gb.gcsescience.com) |
Magnesium juga membentuk klorida ionik. Tidak seperti natrium, magnesium memiliki dua elektron di kulit terluarnya. Kedua elektron tersebut lepas diberikan kepada dua atom klorin. Ion magnesium (Mg2+) membentuk garam dengan formula MgCl2 Magnesium mempunyai valensi dua.
 |
|
Garam Dapur merupakan kristal NaCl (Gb.gcsescience.com) |
Ikatan Kovalen
Senyawa-senyawa ionik terutama terbentuk diantara logam-logam dibagian kiri sistem periodik dan non logam dibagian kanan sistem periodik. Senyawa-senyawa yang hanya mengandung non logam biasanya ditahan dalam molekul oleh atom-atomnya yang bebagi pasangan elektron. Jenis ikatan ini disebut dngan ikatan kovalen.
 |
|
Ikatan Kovalen pada CO2 (Gb.escubes.com) |
Karbon dioksida (CO2) adalah contoh senyawa kovalen. Valensi karbon dan oksigen adalah empat dan dua, karena setiap atom karbon memerlukan empat elektron dan atom oksigen memerlukan dua elektron. Dalam karbon dioksida, satu atom karbon berbagi sepasang elektron dengan setiap dua atom oksigen. dengan cara ini, ketiga atom tersebut melengkapi kulit terluar mereka.
|
Pembentukan iktan kovalen (Gb.escubes.com) |
