Warna dalam kembang api berasal dari berbagai senyawa logam , terutama garam logam. Komponen yang paling penting dari kembang api adalah, tentu saja, mesiu, atau ‘bubuk hitam’ seperti yang juga dikenal. Senyawa ini ditemukan secara kebetulan oleh ahli kimia Cina, yang pada mulanya ingin menemukan obat mujarab dalam kehidupan, mereka menemukan bahwa kombinasi dari madu, sulfur dan sendawa (potasium nitrat) tiba-tiba akan meledak dalam api pada saat pemanasan.

Kombinasi sulfur dan potasium nitrat kemudian bergabung dengan arang di tempat madu, sulfur dan arang berfungsi sebagai bahan bakar dalam reaksi, sementara kalium nitrat berguna sebagai agen pengoksidasi. bubuk hitam modern memiliki perbandingan berat potasium nitrat, arang dan berat sulfur adalah 75:15:10; dan rasio ini tetap tidak berubah sejak sekitar tahun 1781.
Pembakaran bubuk hitam tidak terjadi sebagai reaksi tunggal, sehingga produk dapat lebih rumit. Reaksi yang paling dekat dapat dituliskan dengan persamaan untuk proses ini ditunjukkan di bawah ini, dengan arang disebut dengan rumus empiris:
6 KNO3 + C7H4O + 2 S → K2CO3 + K2SO4 + K2S + 4 CO2 + 2 CO + 2 H2O + 3 N2
Variasi dalam ukuran pelet dari mesiu dan jumlah uap air dapat digunakan untuk secara signifikan untuk meningkatkan waktu pembakaran kembang api.
Seperti bubuk mesiu, kembang api berisi suatu ‘pengikat’ -yang digunakan untuk mengikat komponen bersama-sama, dan juga untuk mengurangi sensitivitas dari goncangan dan tumbukan. Umumnya senyawa pengikat ini terdiri dari senyawa organik, yaitu dekstrin, yang kemudian dapat bertindak sebagai bahan bakar setelah pengapian. Agen pengoksidasi juga diperlukan untuk menghasilkan oksigen yang dibutuhkan untuk membakar campuran, dalam ini biasanya yang digunakan adalah nitrat, klorat, atau perklorat.

Ledakan seperti ‘bintang’ yang terkandung dalam tabung kembang api berisi serbuk logam atau garam yang memberikan warna kembang api. Bahan ini sering dilapisi bubuk mesiu untuk membantu dalam pengapian. Panas yang dilepaskan oleh reaksi pembakaran menyebabkan elektron dalam atom logam menjadi ter eksitasi ke tingkat energi yang lebih tinggi. Bentuk eksitasi ini tidak stabil, sehingga elektron cepat kembali ke energi aslinya (atau keadaan dasar), dan memancarkan kelebihan energi sebagai cahaya. Logam yang berbeda akan memiliki celah energi yang berbeda antara keadaan dasar dan keadaan tereksitasi, yang mengarah ke emisi warna yang berbeda. Ini adalah alasan yang sama persis dengan reaksi nyala api dari logam, bahwa logam yang berbeda memberikan tes api yang berbeda, yang sering kita gunakan untuk membedakan antara logam-logam tersebut. Warna-warna yang dipancarkan oleh logam yang berbeda ditunjukkan pada grafik di bawah ini.
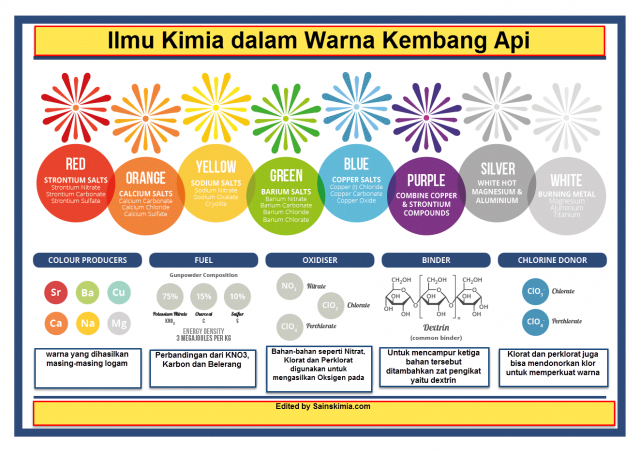
Adanya atom logam dalam senyawa ini sangat penting, maka, tetapi ada beberapa senyawa yang lebih baik daripada senyawa yang lain. senyawa higroskopis (senyawa yang menarik dan menahan air) tidak banyak digunakan dalam kembang api, karena mereka dapat membuat campuran basah dan sulit untuk terbakar. Beberapa warna juga terkenal sulit untuk menghasilkan. Tembaga mengandung senyawa cenderung tidak stabil pada suhu yang lebih tinggi, dan jika mencapai suhu tinggi, akan bertumbukan dan pecah, yang menyebabkan warna biru tidak bisa kelihatan. Untuk alasan ini, itu kita dapat melihat kualitas kembang api dengan cara melihat warna biru yang idhasilkan. Warna ungu juga cukup sulit untuk dihasilkan, karena tetap melibatkan penggunaan senyawa penghasil warna biru yang dikombinasikan dengan bahan yang menyebabkan warna merah.

2 comments