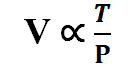Hukum Gas: Definisi, Rumus & Contoh
Hukum gas dikembangkan pada akhir 1800-an ketika para ilmuwan memahami hubungan antara tekanan, volume, dan suhu untuk sampel gas. Hubungan ini, pada gilirannya, akan, kira-kira, berlaku untuk semua gas. Meskipun demikian, semua gas berperilaku serupa. Gas memiliki jarak partikel individu yang luas. ‘Teori Kinetik Gas’ memperoleh ‘Persamaan Keadaan’ untuk gas ideal. Ilmuwan yang berbeda melakukan banyak percobaan dan karenanya, mengajukan hukum gas yang berbeda yang berhubungan dengan variabel keadaan gas yang berbeda.

Variabel keadaan gas adalah:
1. Tekanan, P (mmHg, atm, kPa, dan Torr)
2. Volume, V (L)
3. Suhu, T (K)
4. Jumlah Zat, n
1. Hukum Boyle: Hukum Volume-Tekanan

Hukum Boyle menyatakan bahwa pada suhu konstan, volume suatu massa gas berbanding terbalik dengan tekanan; yaitu, pada suhu konstan V ∝ 1 / P atau PV = konstan.
Bukti: Dari Teori Kinetik gas, kita tahu:
di mana c adalah akar kuadrat rata-rata kecepatan molekul, m1 adalah massa molekul, V adalah volume, dan N adalah jumlah molekul. Sekarang, pada temperatur konstan, c, N, dan m1 adalah konstanta; karenanya,
Saat tekanan meningkat, volume gas berkurang; dan sebaliknya. Persamaan berikut dapat diturunkan dari Hukum Boyle:
Contoh: Saat udara bertekanan diisi ke dalam ban, pengukuran tekanan diperhitungkan. Saat ban mengembang dengan semakin banyak udara pada suhu yang sama, semua molekul gas dipaksa untuk berkumpul bersama, mengurangi volumenya, dan meningkatkan tekanan pada dinding ban.
Contoh lainnya adalah:
Kaleng cat semprot
Jarum suntik
Kaleng soda
2. Hukum Charles: Hukum Suhu-Volume
Hukum Charles atau Hukum Volume menyatakan bahwa pada tekanan konstan, volume suatu massa gas berbanding lurus dengan suhu absolutnya; yaitu, pada tekanan konstan, V ∝ T atau V / T = konstan.
Bukti: Sekarang sebagai c2 ∝ T, jadi pada tekanan konstan untuk massa gas tertentu, V ∝ T.

Dengan meningkatnya suhu gas, volume gas juga meningkat. Selain itu, suhu awal dan akhir, serta volume gas, dapat dengan mudah ditentukan;
Contoh: Meninggalkan bola basket selama bulan-bulan yang dingin akan mengempiskan nya. Kita akan melihat bahwa ketika bola dibiarkan dalam kondisi yang lebih dingin, ia mulai kehilangan udara di dalamnya atau volume nya mulai berkurang. Hal ini membuktikan bahwa dalam kondisi tekanan yang konstan, jika terjadi penurunan suhu maka volume nya juga berkurang
Contoh lengkapnya bisa diliht
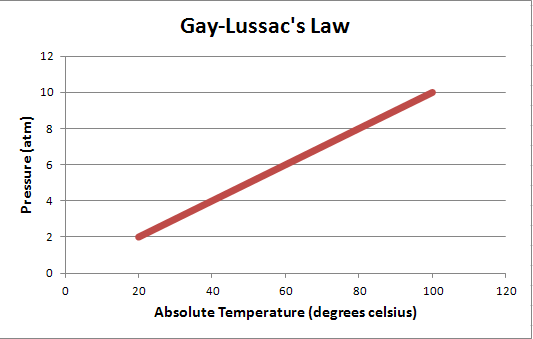
disini3. Hukum Gay Lussac: Hukum Tekanan-Suhu
Hukum Gay Lussac menyatakan bahwa pada volume yang konstan, tekanan suatu massa gas berbanding lurus dengan suhu absolutnya; yaitu, pada volume konstan, P ∝ T atau P / T = konstan.
Bukti: Dari Teori Kinetik gas, kita tahu:
Sekarang sebagai c2 ∝ T, jadi pada volume konstan, P ∝ T untuk massa gas tertentu.
Saat suhu meningkat, tekanan juga meningkat. Dalam kondisi yang sama, tekanan dan suhu awal dan akhir untuk suatu volume gas dapat dihitung;
Contoh:
Cara kerja panci presto mengikuti hukum Gay Lussac. Saat suhu meningkat, tekanan di dalam panci presto juga meningkat, yang membuat makanan lebih cepat matang.
Contoh lainnya adalah:
Ban mobil dalam cuaca panas
Kaleng aerosol
4. Hukum Avogadro: Hukum Jumlah Volume
Hukum Avogadro menyatakan bahwa untuk suhu, tekanan, dan volume yang konstan, semua gas mengandung jumlah molekul yang sama. 1 mol gas Pada STP menempati volume 22,4 L. Penting untuk menentukan hubungan antara jumlah gas (X) dan volume gas (V).
Bukti: Dari Teori Kinetik gas, kita tahu;
Sekarang sebagai c2 ∝ T, jadi pada konstanta V, P, & T, N = konstanta, untuk massa gas tertentu.
Jika jumlah molekul gas meningkat, volume gas juga meningkat;

Jika suhu dan tekanan tetap, fraksi jumlah volume akan konstan;
Contoh: Saat kita menghirup udara, paru-paru akan mengembang. Demikian pula, volume paru-paru menurun saat kita mengeluarkan napas.
Hukum Gas Gabungan
Sekarang, kita dapat dengan mudah menggabungkan hukum Boyle, hukum Charles, dan hukum Guy Lussac menjadi ‘Persamaan Hukum Gas Gabungan’ atau ‘Persamaan Gas Umum’. Ini menentukan hubungan antara tekanan, volume, dan suhu untuk kuantitas tertentu hukum gas gabungan
Volume gas yang diberikan berbanding lurus dengan suhu Kelvin dan berbanding terbalik dengan tekanan.
Volume dan suhu awal dan akhir juga dapat dihitung;
Hukum Gas Ideal
Hukum gas ideal diperoleh dengan menambahkan hukum Avogadro ke hukum gas gabungan:
dimana;
P = tekanan,
V = volume,
n = jumlah mol,
R = konstanta gas universal, 8,3144598 (kPa ∙ L) / (mol ∙ K), dan
T = suhu (K)Formulasi lain dari hukum gas ideal bisa juga dituliskan
dimana,
P = tekanan,
V = volume,
N = jumlah molekul gas,
k = Konstanta Boltzmann, 1,381 × 10−23 J · K − 1 dalam satuan SI, dan
T = suhu (K)
Like this:
Like Loading...